
Inhibidores de Bomba de Protones en Niños
Los inhibidores de la bomba de protones (IBP), como omeprazol, esomeprazol, lansoprazol, pantoprazol y rabeprazol, se encuentran entre los medicamentos recetados con mayor frecuencia en el mundo. Sin embargo, se debate su seguridad con respecto a la salud ósea. Se ha observado recientemente que su uso prolongado particularmente en la población de mayor edad, aumenta la fragilidad ósea.1,2
La terapia con inhibidores de la bomba de protones ha cambiado en forma favorable el tratamiento de las enfermedades gastrointestinales relacionadas con el ácido y sus consecuencias, como la enfermedad por reflujo gastroesofágico, la úlcera péptica y la dispepsia, impactando a su vez en la prevención de las úlceras y hemorragias gástricas.1
Aunque los IBP se consideran un medicamento seguro para el uso terapéutico recomendado, se han descrito una serie de efectos indeseables relacionados a su uso prolongado, incluida la diarrea asociada a Clostridium difficile, neumonía, pero también posiblemente algunos cánceres inducidos por disbiosis intestinal.1
CARACTERÍSTICAS FARMACOLÓGICAS
El tratamiento eficaz con inhibidores de la bomba de protones requiere una comprensión de su farmacocinética. El ATPasa hidrógeno-potasio gástrica es la enzima responsable de la secreción de ácido por parte de la célula parietal en el estómago, después de la estimulación por la unión de diferentes ligandos, como la acetilcolina, la histamina o la gastrina.2
Las moléculas de cisteína (CYS) de la ATPasa hidrógeno-potasio gástrica son accesibles a los IBP para su unión. Para unirse al CYS de la ATPasa, los IBP deben activarse y la velocidad de esta activación varía según sus estructuras. Los inhibidores de la bomba de protones son bases débiles sensibles a los ácidos que requieren un recubrimiento entérico para protegerlos de la destrucción del ácido gástrico y permitir su absorción.2
Los IBP ahora en el mercado tienen una estructura básica que conecta un anillo de benzimidazol y un anillo de piridina a través de un enlace sulfonilo, con numerosas sustituciones en estos anillos que afectan su composición química. Para conectarse químicamente a los CYS de la ATPasa, el sulfonilo debe obtener energía del ambiente ácido dentro de la célula parietal.1,2
Se agregan dos protones a los nitrógenos a ambos lados del grupo sulfonilo para activar el IBP, y una vez activado se puede suprimir la bomba de protones al formar enlaces disulfuro con moléculas CYS en la ATPasa. Para que se inhiba la bomba de protones, el IBP primero debe llegar al sitio de acción dentro de la célula parietal, donde recibirá la activación ácida.2
La farmacocinética de los inhibidores de la bomba de protones determina las concentraciones en el sitio de acción, comenzando por la absorción de la forma inactiva, distribución, procesamiento por el citocromo P450 y aclaramiento. El bloqueo de la bomba de protones requiere la activación de la bomba antes de que el IBP se elimine de la circulación, lo que influye en la tasa de absorción.1,2
Debido a que la producción de gastrina después de una comida es uno de los inductores de ATPasa hidrógeno-potasio gástrica más potentes, el IBP debe tomarse lo suficiente antes de una comida para que se absorba cuando la bomba de protones está más activa. La secreción de ácido se detiene una vez que el IBP activado se une a la ATPasa hidrógeno-potasio gástrica, ya sea de forma reversible o permanente.2
Si te está gustando nuestro contenido esto también te podría interesar: ERGE ALGORITMOS DE TRATAMIENTO Y VENTAJAS DE IBPS
USOS CLÍNICOS EN NIÑOS Y ADOLESCENTES
Los inhibidores de la bomba de protones están autorizados para uso en niños mayores de 1 año, para el tratamiento de ERGE a corto plazo, esofagitis erosiva, tratamiento de la úlcera péptica y erradicación del Helicobacter pylori. También se consideran el estándar de atención para la esofagitis eosinofílica pediátrica.1,2
Una revisión sistemática que incluye 12 estudios sobre el uso de IBP (esomeprazol, lansoprazol, omeprazol y pantoprazol) en niños con ERGE identificó cuatro ensayos en los que los IBP fueron más efectivos para la acidez gástrica que el placebo, los ácidos algínicos o la ranitidina.2
En tres de los estudios, los IBP no mostraron diferencias significativas con respecto a la ranitidina o los alginatos en la reducción de las alteraciones histológicas. Un estudio multicéntrico, doble ciego, de grupos paralelos mostró que el rabeprazol es eficaz en niños de 1 a 11 años de edad con ERGE asignados al azar para recibir 0,5 o 1,0 mg/kg de rabeprazol durante 12 semanas, con más ajuste de dosis por peso.2
Los mismos autores han determinado adicionalmente la eficacia del tratamiento de mantenimiento con rabeprazol en niños de 1 a 11 años que padecen ERGE, mostrando un mantenimiento de la cicatrización en el 90% de los niños. En niños con síntomas típicos de ERGE, las guías pediátricas actuales recomiendan una prueba de IBP de 4 a 8 semanas.2
La farmacodinámica de los IBP para el tratamiento de los trastornos del ácido péptico en niños de 1 año o más, es comparable a la de los pacientes adultos. En un estudio aleatorizado realizado en niños de 1 a 11 años de edad con esofagitis erosiva, el tratamiento con IBP (0,2 a 1,0 mg/kg de esomeprazol) condujo a la curación de las erosiones en el 89% de los casos después de 8 semanas de tratamiento.2
En el caso de la infección por Helicobacter pylori, los inhibidores de la bomba de protones también se recomiendan para la terapia de erradicación de segunda línea. La dosis de IBP utilizada para la terapia en niños es la siguiente tabla:
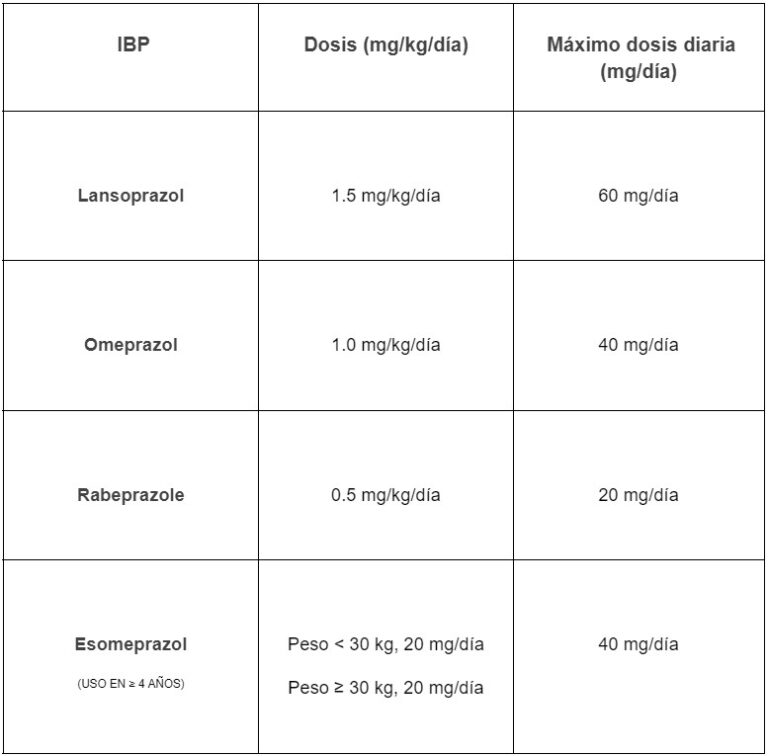
La esofagitis eosinofílica pediátrica es una causa inmunomediada de inflamación esofágica con tasas de incidencia y prevalencia de 5,1 casos/100.000 personas/año. Inicialmente, los IBP se utilizaron para diferenciar la esofagitis eosinofílica pediátrica de la eosinofilia esofágica que responde a los IBP, que se pensaba que estaba relacionada con la enfermedad por reflujo gastroesofágico.2
De acuerdo a diversos estudios europeos sobre esofagitis eosinofílica pediátrica, la terapia con inhibidores de la bomba de protones ya no es necesaria para el diagnóstico, y se puede considerar como parte del manejo terapéutico. Varios ensayos controlados aleatorios prospectivos respaldan la eficacia de la terapia con IBP para inducir la remisión de la esofagitis eosinofílica pediátrica.2
Contrariamente a las indicaciones en niños mayores, las indicaciones para el uso de inhibidores de la bomba de protones en lactantes son menos claras. El esomeprazol es el único IBP aprobado para su uso en pacientes de 1 mes a menores de 12 meses de edad. Las recomendaciones son consistentes con la evidencia disponible de que los IBP no son efectivos para tratar los síntomas generalmente atribuidos a ERGE en bebés por lo demás sanos, como llanto inexplicable, irritabilidad o trastornos del sueño.2
SEGURIDAD EN EL USO DE INHIBIDORES DE LA BOMBA DE PROTONES
Un estudio retrospectivo reciente encontró 70 informes de efectos adversos de los inhibidores de la bomba de protones en niños, la mayoría de los cuales no eran graves o irreversibles, siendo las manifestaciones gastrointestinales (24%) y cutáneas (21,3%) las más frecuentes.1,2
En términos de efectos secundarios a corto plazo, el 34% de los niños que usan IBP experimentan cefaleas, náuseas, diarrea o estreñimiento. En los niños, el uso crónico de IBP se ha asociado con un mayor riesgo de infecciones gastrointestinales y del tracto respiratorio, fracturas óseas y alergias. Aunque se desconoce el perfil de toxicidad de los IBP, se han propuesto vías patogénicas que están principalmente conectadas a la supresión de ácido gástrico a largo plazo.1,2
INFECCIONES
Varios estudios en adultos han encontrado un posible vínculo entre los IBP y un mayor riesgo de infecciones entéricas, pero solo unos pocos estudios en niños han investigado esto. La infección por Clostridium difficile es la infección más comúnmente discutida relacionada con el uso de inhibidores de la bomba de protones.2
En un análisis retrospectivo reciente de 124 niños (de 1 a 18 años) que tenían diarrea y dieron positivo para Clostridium difficile, se encontró que 49 niños tenían infección por Clostridium difficile y 75 niños tenían colonización. Curiosamente, la edad mayor de 4 años y el uso de IBP fueron las variables independientes para enfermedades graves entre los pacientes con la infección.2
FRACTURAS ÓSEAS
Los datos sobre el riesgo de osteoporosis y fracturas óseas provienen principalmente de adultos. En un estudio basado en la población que incluyó 124 799 casos entre las edades de 4 a 29 años, se encontró un mayor riesgo de fracturas en adultos jóvenes (18 a 29 años) con IBP, pero no en niños.1,2
En comparación con los controles, los niños que recibieron tratamiento de supresión de ácido antes de cumplir un año tenían una mediana de edad más temprana en la primera fractura (3,8 frente a 4,5 años) en una cohorte retrospectiva de pacientes seguidos durante 2 años. La supresión de ácido antes de la edad de un año y la terapia durante un período más prolongado se relacionaron con un mayor riesgo de fractura.1,2
Vertismed de Tecnofarma es una plataforma innovadora de contenido Médico Científico, donde los profesionales de la salud podrán aprender constantemente y mantenerse actualizados sobre las distintas especialidades médicas, con la finalidad de adquirir nuevos conocimientos e impulsar su carrera profesional. Regístrate ingresando a nuestra web y se parte de la innovación médica.
REFERENCIAS BIBLIOGRÁFICAS:
- Lespessailles, E., & Toumi, H. (2022). Proton pump inhibitors and bone health: An update narrative review. International Journal of Molecular Sciences, 23(18), 10733. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9504265/
- Dipasquale, V. Cicala, G. Spina, E. Romano, C. (2022) A Narrative Review on Efficacy and Safety of Proton Pump Inhibitors in Children. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8866943/
Este material fue revisado y aprobado por el Departamento Médico de Tecnofarma Perú.
0523_LANZOPRAZOLEZOMEPRAZOLOMEPRAZOLARTICULODIG_OES




Lo sentimos, el formulario de comentarios está cerrado en este momento.