Terapia de deprivación androgénica en pacientes con cáncer de próstata resistente a la castración y Triptorelina: como tratamiento hormonal del cáncer de próstata
La supresión androgénica (TDA) es el pilar del tratamiento del cáncer de próstata durante el transcurso de los diferentes estadíos de la enfermedad, principalmente en los pacientes metastásicos. Existen diferentes estrategias para logar valores circulantes de testosterona
en castración, definido por las diferentes guías de práctica clínica en un valor de <50 ng/dl1-3. Los agonistas de la hormona liberadora de gonadotrofina (GnRH) como triptorelina pertenecen al grupo de medicamentos que permiten alcanzar este objetivo4.
Los pacientes con enfermedad avanzada, luego de iniciado el tratamiento de TDA y en tiempo variable, progresan al estado de castración resistencia (CPCR), donde la enfermedad desarrolla diferentes mecanismos de adaptación. La enfermedad progresa a pesar de mantener niveles de testosterona en castración, y la vía androgénica continúa siendo el principal mecanismo fisiopatológico para el desarrollo de la enfermedad. Mecanimos como la síntesis de testosterona por parte del tumor es suficiente para activar a los receptores de andrógenos, por lo tanto, mantener niveles bajos de testosterona circulante continúa siendo importante aún en esta situación5.
Actualmente hay un gran número de tratamientos con demostrado beneficio en pacientes con CPCR, tanto en la situación de enfermedad metastásica (abiraterona6, enzalutamida7, docetaxel8, cabazitaxel9, radium 22310) como en enfermedad no metastásica (apalutamida11,
enzalutamida12, darolutamida13). Todos los estudios clínicos pivotales que evaluaron estas alternativas de tratamiento continuaron con la TDA.
Hay evidencia de que la utilización de nuevos antiandrógenos como abiraterona en monoterapia no logran un estado de castración persistente14 y el agregado de TDA a este tratamiento resulta en un descenso sostenido y más profundo de los niveles de testosterona
y de la concentración de esteroides adrenales15 con impacto significativo en el beneficio del tratamiento. Todos los estudios Fase III de enzalutamida en pacientes en diferentes situaciones de enfermedad continúan con la TDA para mantener un nivel circulante de testosterona en castración, esto y el potencial evento adverso de ginecomastia reportado con la utilización de enzalutamida en monoterapia sugieren que el tratamiento de supresión hormonal debe continuar en los pacientes con CPCR. En los pacientes con CPCS no metastásicos, los beneficios en intervalo libre de metástasis y supervivencia global obtenidos con enzalutamida, darolutamida y apalutamida se obtienen manteniendo la TDA durante toda la evolución de enfermedad. El tratamiento conjunto de quimioterapia, como docetaxel o cabacitaxel logra mejores beneficios con el uso conjunto de TDA.
Por esta razón hay evidencia suficiente de continuar con terapias que logren valores de testosterona en castración en los pacientes con CPCR, en conjunto con terapias con demostrado beneficio. Triptorelina es una
opción efectiva y segura, para lograr estos objetivos.
Referencias:
1. EAU – ESTRO – ESUR – SIOG Guidelines on Prostate Cancer. Available from: http://uroweb.org/guideline/prostate-cancer/ (Access Date: February 2018. No Title.
2. Scher HI, Morris MJ, Stadler WM, et al. The Prostate Cancer Working Group 3 (PCWG3) consensus for trials in castration-resistant prostate cancer (CRPC). J Clin Oncol. 2015;33(15_suppl):5000. doi:10.1200/jco.2015.33.15_suppl.5000.
3. Mottet N, van den Bergh RCN, Briers E, et al. EAU – ESTRO – ESUR – SIOG Guidelines on Prostate Cancer 2018. In: European Association of Urology Guidelines. 2018 Edition. Vol presented. Arnhem, The Netherlands: European Association of Urology Guidelines Office; 2018. http://uroweb.org/guideline/prostate-cancer/ LK – Prostate Cancer Uroweb%7Chttp://uroweb.org/guideline/prostate-cancer/%7C FG – 0.
4. Merseburger AS, Hupe MC. An Update on Triptorelin: Current Thinking on Androgen Deprivation Therapy for Prostate Cancer. Adv Ther. 2016;33(7):1072-1093. doi:10.1007/s12325-016-0351-4.
5. Merseburger A, Hammerer P, Rozet F, et al. Androgen deprivation therapy in castrate-resistant prostate cancer: how important is GnRH agonist backbone therapy? World J Urol. 2014;33. doi:10.1007/s00345-014-1406-2.
6. Fizazi K, Scher HI, Molina A, et al. Abiraterone acetate for treatment of metastatic castration-resistant prostate cancer: final overall survival analysis of the COU-AA-301 randomised, double-blind, placebo-controlled phase 3 study. Lancet Oncol. 2012;13(10):983-992. doi:10.1016/S1470-2045(12)70379-0
7. Evans CP, Higano CS, Keane T, et al. The PREVAIL Study: Primary Outcomes by Site and Extent of Baseline Disease for Enzalutamide-treated Men with Chemotherapy-naïve Metastatic Castration-resistant Prostate Cancer. Eur Urol. 2016;70(4):675-683. doi:10.1016/j.eururo.2016.03.017.
8. Petrylak DP, Tangen CM, Hussain MHA, et al. Docetaxel and Estramustine Compared with Mitoxantrone and Prednisone for Advanced Refractory Prostate Cancer. N Engl J Med. 2004;351(15):1513-1520. doi:10.1056/NEJMoa041318.
9. Oudard S, Fizazi K, Joly F, et al. Cabazitaxel in metastatic castration-resistant prostate cancer (mCRPC): Real-life use, effectiveness, safety, and quality of life (QoL) in the FUJI cohort. J Clin Oncol. 2018;36(15_suppl):5025. doi:10.1200/JCO.2018.36.15_suppl.5025.
10. Parker C, Nilsson S, Heinrich D, et al. Alpha Emitter Radium-223 and Survival in Metastatic Prostate Cancer. N Engl J Med. 2013;369(3):213-223. doi:10.1056/NEJMoa1213755.
11. Smith MR, Saad F, Chowdhury S, et al. Apalutamide Treatment and Metastasis-free Survival in Prostate Cancer. N Engl J Med. 2018;378(15):1408-1418. doi:10.1056/NEJMoa1715546.
12. Hussain M, Fizazi K, Saad F, et al. Enzalutamide in Men with Nonmetastatic, Castration-Resistant Prostate Cancer. N Engl J Med. 2018;378(26):2465-2474. doi:10.1056/NEJMoa1800536.
13. Fizazi K, Shore N, Tammela TL, et al. Darolutamide in Nonmetastatic, Castration-Resistant Prostate Cancer. N Engl J Med. 2019;380(13):1235-1246. doi:10.1056/NEJMoa1815671.
14. Ryan CJ, Peng W, Kheoh T, et al. Androgen dynamics and serum PSA in patients treated with abiraterone acetate. Prostate Cancer Prostatic Dis. 2014;17(2):192-198. doi:10.1038/pcan.2014.8.
15. O’Donnell A, Judson I, Dowsett M, et al. Hormonal impact of the 17alphahydroxylase/C(17,20)-lyase inhibitor abiraterone acetate (CB7630) in patients with prostate cancer. Br J Cancer. 2004;90(12):2317-2325. doi:10.1038/sj.bjc.6601879.
Triptorelina: su rol como tratamiento hormonal del cáncer de próstata
La terapia de deprivación androgénica (TDA) ha sido el pilar del tratamiento en los pacientes con cáncer de próstata avanzado desde hace ya décadas. El objetivo de la TDA es reducir los niveles de testosterona alcanzados por la castración quirúrgica, definidos como ≤50
ng/dL (≤1.7 nmol/L)1. El tratamiento con TDA está recomendado en pacientes con tumores localizados de alto riesgo en conjunto con el tratamiento radiante, de forma adyuvante en pacientes con márgenes positivos o persistencia de enfermedad ganglionar luego de la
cirugía, en pacientes seleccionados con recaída bioquímica y pacientes con metástasis a distancia1. La supresión de los valores de testosterona puede lograrse a través de diferentes estrategias, siendo los agonistas del receptor de GnRH el tratamiento más frecuentemente utilizado en la práctica clínica.
Triptorelina es un agonista de GnRH con probada eficacia y seguridad a partir de la evidencia de los estudios clínicos y su uso en la práctica habitual. La administración de la formulación de liberación prolongada inicialmente estimula la secreción de LH y FSH por parte de la hipófisis, con aumento de los niveles de testosterona2 transitorio, y un descenso marcado posterior bajo la exposición continua de triptorelina.
Existe una sólida evidencia que respalda la eficacia y seguridad de triptorelina en el tratamiento del cáncer de próstata localmente avanzado y metastásico.
Los pacientes tratados con triptorelina de forma continua alcanzan el objetivo de supresión androgénica (testosterona circulante ≤50 ng/dL o ≤1.7 nmol/L), logrando en la mayor parte de los pacientes valores de testosterona aun más bajos (≤20 ng/dL) lo que sabemos que tiene un impacto significativo en la respuesta de la enfermedad. La efectividad de este tratamiento fue demostrada en diferentes formulaciones, tales como en dosis de 3.75 mg mensual y 11.25 mg cada 3 meses3,4. Los valores de castración son alcanzados a los 28 días de tratamiento en el 91.2% de los pacientes tratados5. Se demostró que la efectividad en lograr la supresión androgénica se mantiene en el tiempo donde un 98.3% continúan en castración luego de 12 meses 6.
Las diferentes formulaciones de triptorelina han demostrado lograr valores más profundos de supresión andrógenica, 90% de los pacientes lograron valores de testosterona circulante de 20 ng/dL a los 6, 9 y 12 meses luego de la aplicación intramuscular7. La definición más riguro-
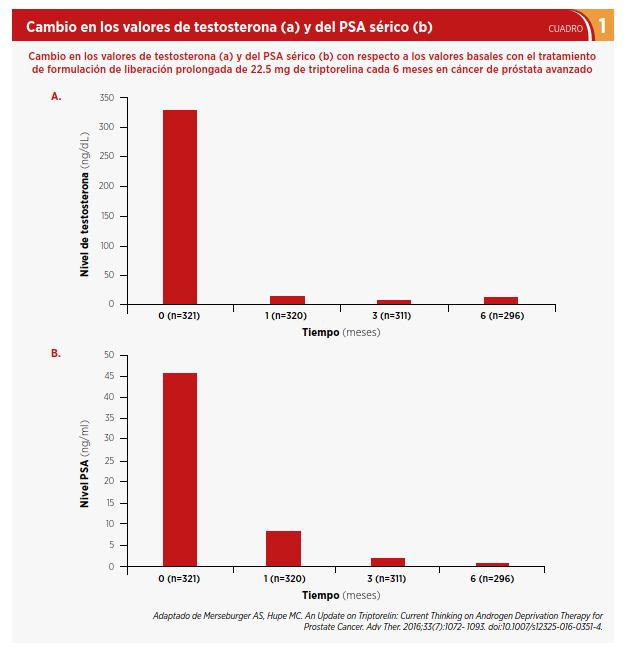
sa de castración no ha sido ampliamente adoptada por las guías de práctica clínica, pero existe evidencia de que se observan mejores resultados si se alcanzan niveles de testosterona <50 ng/dL8. Esta reducción significativa en los valores de testosterona circulante coincide con una
mayor disminución de los valores del PSA y respuesta de la enfermedad (ver Cuadro 1).
Existe suficiente evidencia que respalda que, la triptorelina, aplicada de forma mensual o trimestral mejora los síntomas del tracto genitourinario inferior de forma significativa luego de 6 y 12 meses de tratamiento. Esta mejoría sintomática se correlaccionó con los niveles de
PSA9. La eficacia de triptorelina en los estudios clínicos se comprobó en numerosos estudios de pacientes en la práctica habitual.
El tratamiento con triptorelina es generalmente bien tolerado. Los eventos adversos más frecuentes con las formulaciones intramusculares y subcutáneas son similares a los observadas con otros agonistas GnRH tales como sofocos, disfunción eréctil, disminución de la libido6. La
discontinuación del tratamiento secundaria a eventos adversos relacionados con la droga es infrecuente 6.
La supresión androgénica es el pilar del tratamiento del cáncer de próstata avanzado, donde los agonistas de GnRH son la opción más utilizada. Triptorelina es un agonista de GnRH indicado como primera maniobra hormonal en pacientes con cáncer de próstata localmente avanzado y metastásico. La disponibilidad de formulaciones de liberación prolongada por vía in-tramuscular y subcutánea, ofrece flexibilidad y conveniencia para los pacientes. Estas formulaciones tienen comprobada eficacia y seguridad en estudios clínicos y en la práctica del mundo real.
.
Referencias:
1. Merseburger AS, Hupe MC. An Update on Triptorelin: Current Thinking on Androgen Deprivation Therapy for Prostate Cancer. Adv Ther. 2016;33(7):1072-1093. doi:10.1007/s12325-016-0351-4
2. https://www.medicines.org.uk/emc/medicine/24154. No Title.
3. Abbou CC, Lucas C, Leblanc V. [Tolerance and clinical and biological responses during the first 6 months of treatment with 1-month sustained release LHRH agonists leuprolerin and triptolerin in patients with metastatic prostate cancer]. Prog en Urol J l’Association Fr d’urologie la Soc Fr d’urologie. 1997;7(6):984-995.
4. Minkov NK, Zozikov BI, Yaneva Z, Uldry PA. A phase II trial with new triptorelin sustained release formulations in prostatic carcinoma. Int Urol Nephrol. 2001;33(2):379-383. doi:10.1023/a:1015274031704
5. Heyns CF, Simonin M-P, Grosgurin P, Schall R, Porchet HC. Comparative efficacy of triptorelin pamoate and leuprolide acetate in men with advanced prostate cancer. BJU Int. 2003;92(3):226-231. doi:10.1046/j.1464-410x.2003.04308.x
6. Lundström EA, Rencken RK, van Wyk JH, et al. Triptorelin 6-month formulation in the management of patients with locally advanced and metastatic prostate cancer: an open-label, non-comparative, multicentre, phase III study. Clin Drug Investig. 2009;29(12):757-765. doi:10.2165/11319690-000000000-00000
7. Ploussard G, Mongiat-Artus P. Triptorelin in the management of prostate cancer. Future Oncol. 2013;9(1):93-102. doi:10.2217/fon.12.158
8. https://uroweb.org/guideline/prostate-cancer/. No Title.
9. Gil T, Aoun F, Cabri P, Maisonobe P, van Velthoven R. A prospective, observational grouped analysis to evaluate the effect of triptorelin on lower urinary tract symptoms in patients with advanced prostate cancer. Ther Adv Urol. 2015;7(3):116-124. doi:10.1177/1756287215574480




Lo sentimos, el formulario de comentarios está cerrado en este momento.